多总管
12 月 25 日,赛诺菲 Dupilumab 注射液的上市申请获药审中心承办(受理号:JXSS1900067)
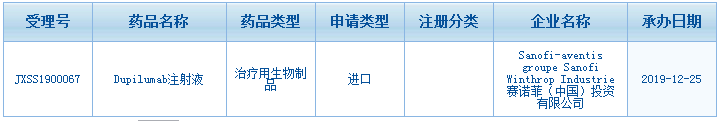
Dupiluma 是一种人源性单克隆抗体,用于治疗哮喘和过敏性皮炎的白细胞介素-4(IL-4)受体阻断剂。由赛诺菲和再生元共同研发。
2014年,Dupilumab被美国FDA认证为治疗特应性皮炎的突破性疗法。
2017 年 3 月 28 日, Dupixent®获 FDA 批准上市,成为首个治疗中重度特应性皮炎的生物制剂。

药智数据库显示,Dupixent 目前在全球正在开展多项临床试验,其中在国内,Dupilumab 用于中重度特应性皮炎成年患者的 3 期临床正在进行中(临床登记号:CTR20181386),计划入组 160 人。
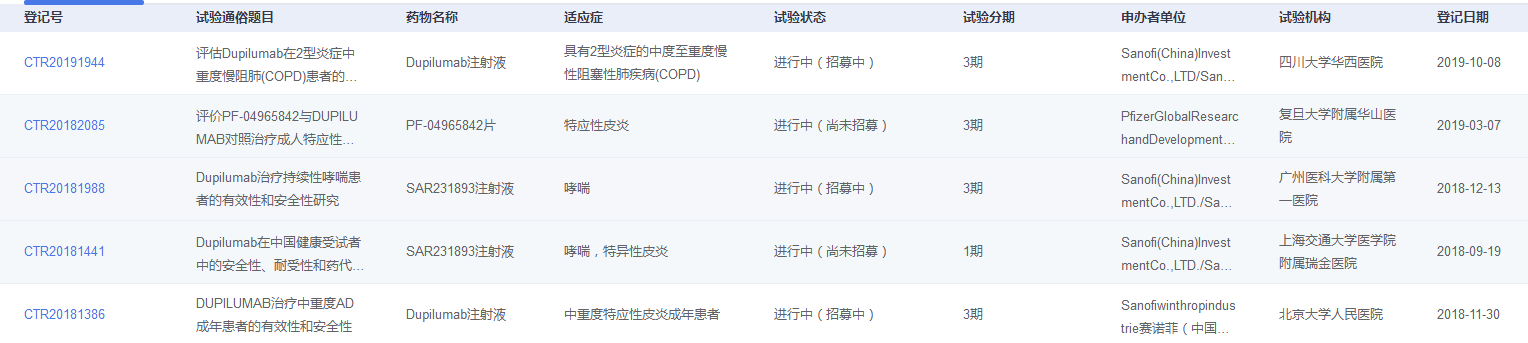
治疗慢阻肺(COPD)的国际多中心 3 期临床也在进行中(临床登记号:CTR20191944),计划入组人数:国际多中心试验:总体924人,中国82人。
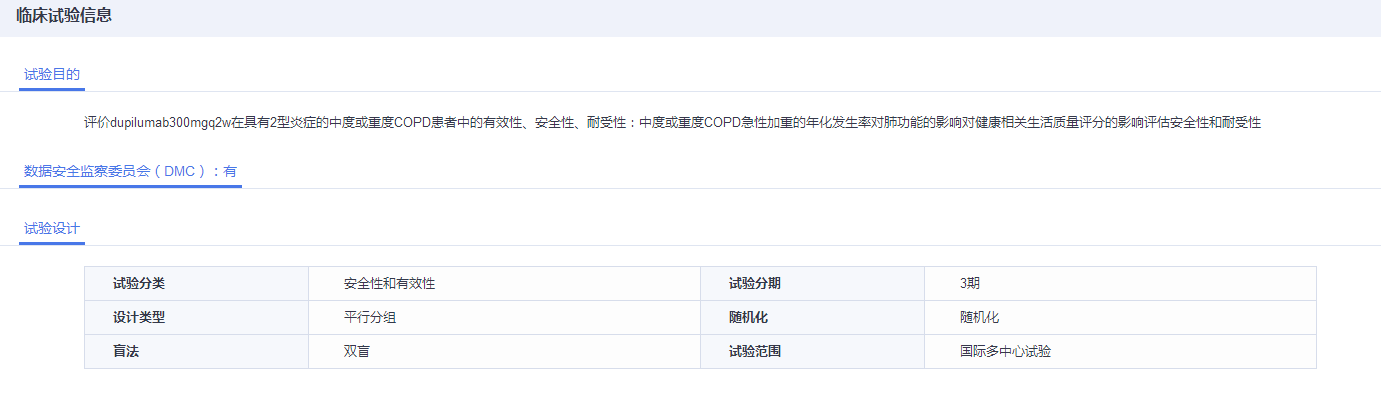
目前,Dupixent 已在包括美国、日本、欧盟约 40 个国家和地区获得监管机构批准并上市。2017年上市到2018 年销售额跨越式增长。
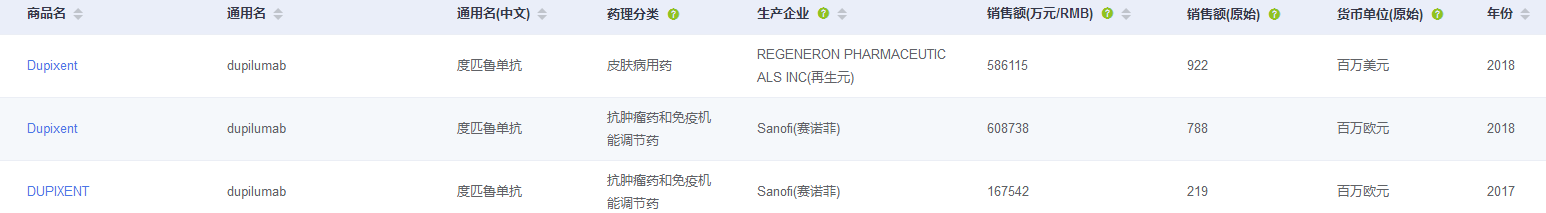
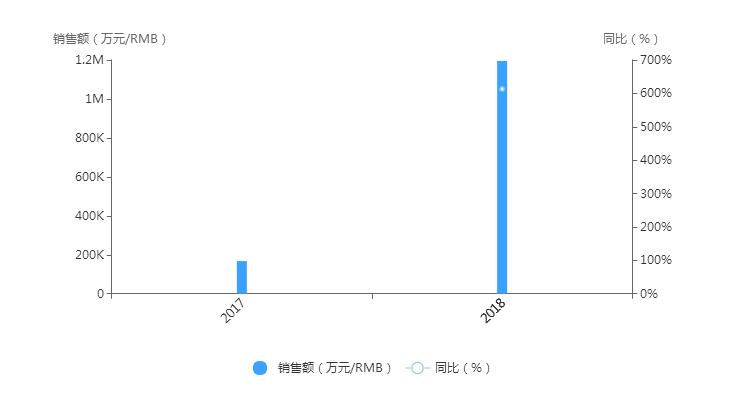
随着其临床适应症的不断增加以及市场的不断扩张,该药在未来将成为继艾伯维修美乐之后的全球第二大畅销抗炎药。
来源于:药智网