多总管
百济神州公布2019年第三季度财务业绩。
2019年11月13日,百济神州公司今天公布近期业务亮点、预计里程碑事件、以及2019年第三季度财务业绩。
百济神州创始人、首席执行官兼董事长欧雷强先生表示:“近期,我们与安进公司宣布建立了一项变革型的合作,预计将于2020年初完成。届时,我们将开始执行针对安进公司三款商业阶段药物和20款候选药物在中国的商业化和开发计划。我们相信此次合作更加巩固了我们作为在中国商业化和开发首选伙伴的地位,而这一切都是因为在我们的人才、全球影响,以及对患者、合规和质量坚定的承诺上。在过去的一个季度中,我们继续筹备在美国和中国计划中的产品上市。展望公司在今年年底前和2020年的各项重要事件,共有多至10项正在开展的3期或潜在的注册性临床试验计划公布数据,同时还有计划中的两款公司自主开发产品的商业上市。”
近期业务亮点以及预计里程碑事件
临床项目
泽布替尼,一款设计旨在最大化布鲁顿酪氨酸激酶(BTK)占有率、最小化脱靶效应的在研BTK小分子抑制剂
宣布了美国食品药品监督管理局(FDA)已受理泽布替尼用于治疗复发/难治性(R/R)套细胞淋巴瘤(MCL)患者的新药上市申请(NDA)并授予优先审评资格,《处方药申报者付费法案》(PDUFA)日期为2020年2月27日;
启动了以下临床试验:
一项泽布替尼联合利妥昔单抗对比苯达莫司汀联合利妥昔单抗用于治疗既往未接受过治疗且不适合干细胞移植的MCL患者的全球3期临床试验(clinicaltrials.gov登记号:NCT04002297);
一项用于治疗既往接受过治疗并对伊布替尼治疗不耐受的慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)患者的全球2期临床试验(clinicaltrials.gov登记号:NCT04116437)。
泽布替尼预计里程碑事件
于第61届美国血液学协会(ASH)年会(2019年12月7-10日在美国奥兰多市举行)上公布泽布替尼对比苯达莫司汀联合利妥昔单抗用于治疗既往未经治疗的CLL/SLL患者的SEQUOIA3期临床试验中染色体17p缺失患者分组的初步数据;一项用于治疗R/RCLL/SLL患者的1/2期临床试验更新数据;泽布替尼联合替雷利珠单抗用于治疗B细胞恶性淋巴肿瘤患者的临床试验更新结果;
于2019年公布泽布替尼对比伊布替尼用于治疗华氏巨球蛋白血症(WM)患者的ASPEN全球3期临床试验主要数据;
在美国获得FDA用于治疗R/RMCL患者的新药上市批准,目前PDUFA日期为2020年2月27日;
于2020年上半年在中国获得用于治疗R/RMCL患者以及R/RCLL/SLL患者的新药上市批准;
于2020年上半年在中国递交用于治疗WM患者的新适应症申请(sNDA);
最早于2020年公布SEQUOIA临床试验主要数据;
于2019年或2020年初完成泽布替尼对比伊布替尼用于治疗R/RCLL/SLL患者的ALPINE3期临床试验的患者入组以及泽布替尼用于治疗R/R边缘区淋巴瘤(MZL)患者的MAGNOLIA2期临床试验的患者入组。
替雷利珠单抗,一款设计旨在避免与巨噬细胞中Fc受体结合的、针对免疫检查点受体PD-1的在研人源化IgG4单克隆抗体
完成替雷利珠单抗对比索拉非尼用于治疗一线不可切除肝细胞癌(HCC)患者的全球3期临床试验(clinicaltrials.gov登记号:NCT03412773)的患者入组;
在欧洲肿瘤内科学会(ESMO)2019年大会上公布了在中国和韩国开展的替雷利珠单抗用于治疗局部晚期或转移性尿路上皮癌(UC)患者的2期临床试验(clinicaltrials.gov登记号:NCT04004221)数据;
在第22届中国临床肿瘤学会(CSCO)年会上公布了以下临床数据:
在中国开展的一项替雷利珠单抗联合化疗用于治疗一线肺癌患者的2期临床试验(clinicaltrials.gov登记号:NCT03432598)结果;
在中国开展的一项替雷利珠单抗联合化疗用于治疗ESCC患者的2期临床试验(clinicaltrials.gov登记号:NCT03469557)的更新结果;
在中国开展的一项替雷利珠单抗用于治疗晚期实体瘤患者的1/2期临床试验(药物临床试验登记号:CTR20160872)。
替雷利珠单抗预计里程碑事件
于2019年在中国获得用于治疗R/R经典型霍奇金淋巴瘤(cHL)患者的新药上市批准;
于2020年在中国获得用于治疗局部晚期或转移性UC患者的新适应症上市批准;
于2019或2020年初就替雷利珠单抗用于治疗二、三线HCC患者的全球2期临床试验(clinicaltrials.gov登记号:NCT03419897)的初步结果与药品监管机构沟通;
于2020年公布在中国开展的替雷利珠单抗联合化疗对比化疗用于治疗一线鳞状非小细胞肺癌(NSCLC)患者的3期临床试验(clinicaltrials.gov登记号:NCT03594747)主要数据;
于2020年公布在中国开展的替雷利珠单抗联合化疗对比化疗用于治疗一线非鳞状NSCLC患者的3期临床试验(clinicaltrials.gov登记号:NCT03663205)的主要数据;
于2019或2020年初完成替雷利珠单抗对比多西他赛用于治疗二线NSCLC患者的3期临床试验(clinicaltrials.gov登记号:NCT03358875)全球部分的患者入组;于2020年上半年完成替雷利珠单抗对比化疗用于治疗二线晚期ESCC患者的全球3期临床试验(clinicaltrials.gov登记号:NCT03430843)的患者入组。
Pamiparib,一款在研小分子PARP抑制剂
在ESMO大会上公布了以下临床数据:
Pamiparib联合低剂量替莫唑胺用于治疗局部晚期或转移性实体瘤患者的1b期临床试验(clinicaltrials.gov登记号:NCT03150810)的更新结果;
Pamiparib用于治疗晚期实体瘤患者的1期临床试验(clinicaltrials.gov登记号:NCT02361723)剂量递增/拓展的更新结果。
Pamiparib预计里程碑事件
于2020年就在中国开展的pamiparib用于治疗既往接受过治疗的卵巢癌(OC)患者的关键性2期临床试验(clinicaltrials.gov登记号:NCT03333915)的初步结果与药品监管机构沟通;
于2020年公布pamiparib用于铂敏感复发性OC患者维持治疗的3期临床试验(clinicaltrials.gov登记号:NCT03519230)的数据;
于2020年公布一项pamiparib用于治疗OC患者的全球1期临床试验(clinicaltrials.gov登记号:NCT02361723)数据,以及pamiparib联合替雷利珠单抗用于治疗晚期实体瘤患者的1期临床试验(clinicaltrials.gov登记号:NCT02660034)更新数据;
于2020年在中国递交针对OC的NDA。
Lifirafenib(BGB-283),一款在研RAF二聚体抑制剂
联合SpringWorksTherapeutics启动了一项lifirafenib联合MEK抑制剂mirdametinib(PD-0325901)用于治疗晚期或难治性实体瘤患者的临床试验(clinicaltrials.gov登记号:NCT03905148)。
BGB-A1217,一款在研TIGIT单克隆抗体
启动了在中国和澳大利亚开展的一项以研究联合用药安全性、耐受性、药代学以及初步抗肿瘤活性为目的的BGB-A1217联合替雷利珠单抗用于治疗晚期实体瘤患者的1a/1b期临床试验(clinicaltrials.gov登记号:NCT04047862)的患者入组。
BGB-11417,一款在研小分子Bcl-2抑制剂
完成了BGB-11417临床前以及支持新药研究申请(IND)的研究,在对抗促凋亡蛋白Bcl-2中展示了强效活性与高选择性。
BGB-11417预计里程碑事件
于2020年上半年在澳大利亚和美国启动一项评估BGB-11417在成熟B细胞恶性肿瘤中的安全性、耐受性、药代动力学以及初步抗肿瘤活性的1期临床研究。
生产基地
位于中国广州的生物药品生产基地完成一期项目建设与生产设备确认验证,并正式开始运营。
商业运营
在中国,瑞复美®用于治疗R/R多发性骨髓瘤患者被正式纳入国家医保目录(NRDL);
在中国,替雷利珠单抗用于治疗R/RcHL患者计划中的产品上市准备工作正在继续开展,医药销售人员培训已经完成;
在美国,已经招募医药销售人员,积极筹备计划中的泽布替尼用于治疗R/RMCL患者的产品上市。
公司发展
宣布与安进公司建立全球肿瘤战略合作关系,在中国开发和商业化安加维®(XGEVA®)地舒单抗注射液、KYPROLIS®注射用卡非佐米和BLINCYTO®注射用倍林妥莫双抗,同时共同开发20款安进抗肿瘤管线药物。安进已同意购入约27亿美元的百济神州股份。该交易在符合以下条件的情况下预计将于2020年初完成:百济神州根据香港联合交易所上市规定获得多数股东批准、根据适用的反垄断法的等待期到期或终止、以及满足其他特定交割条件。公司持有约40%股份的股东已同意对该交易投赞成票;
宣布与SeattleGenetics就一款先进的临床前肿瘤候选药物达成全球许可协议,百济神州获得在亚洲(除日本以外)、除美洲(美国、加拿大以及拉丁美洲国家)和欧洲以外全球其他地区的开发和商业化权利。该候选药物运用SeattleGenetics专利保护的抗体技术,预计将于2020年上半年进入临床试验阶段。
2019年第三季度财务业绩
现金、现金等价物、受限资金和短期投资截至2019年9月30日,公司持有的现金、现金等价物、受限资金和短期投资为12.8亿美金,相比较,2019年6月30日的持有额为15.6亿美金,2018年12月31日的持有额为18.1亿美金。
截至2019年9月30日的第三季度,经营活动所用2.6501亿美元,相比较,2018年同期经营活动所用1.3219亿美元。增加主要归因于用于支持美国和中国后期候选药物产品发布准备不断提升的运营费用、公司内部以及授权候选药物的持续开发以及公司整体规模扩大。
截至2019年9月30日的第三季度,资本开支为3087万美元,主要归因于广州生物制剂生产基地建设。
收入截至2019年9月30日的第三季度收入为5014万美元,相比较,2018年同期的收入为5420万美元。收入减少主要归因于2019年第二季度中新基公司就终止替雷利珠单抗合作所支付的相关费用,以及因此停止的任何相关合作收入。
截至2019年9月30日的第三季度,ABRAXANEP®P、瑞复美及维达莎P®P在中国销售带来的产品收入总计5014万美元,相比较,去年同期的产品收入总计为3845万美元。2019年第三季度销售额受到ABRAXANE临时供应中断的负面影响。
截至2019年9月30日的第三季度,合作收入为零,相比较,2018年同期的合作收入为1576万美元。合作收入的减少主要归因于2019年第二季度中新基公司终止了关于替雷利珠单抗的合作。
费用截至2019年9月30的第三季度费用为3.6241亿美元,相比较,2018年同期的费用为2.053亿美元。
销售成本截至2019年9月30日的第三季度为2011万美元,相比较,2018年同期的销售成本为871万美元。销售成本包括这一时期在中国获得ABRAXANE、瑞复美与维达莎销售权益的取得成本。为商业化上市准备产生的库存生产成本,在上市批准之前都计入研发费用。
研发(R&D)费用截至2019年9月30日的第三季度为2.3697亿美元,相比较,2018年同期的研发费用为1.4759亿美元。增加主要归因于正在开展和新启动的后期关键性临床试验费用的持续增加、注册申报准备,以及产品上市前活动和供应相关的生产成本。研发费用的总体增加还归因于员工股权奖励支出的增加,截至2019年9月30日的第三季度股权奖励支出为2067万美元,相比较,2018年同期的股权奖励支出为1552万美元。该增加主要由于员工人数的增长。
销售、一般及行政管理(SG&A)费用截至2019年9月30日的第三季度的销售、一般及行政管理费用为1.05亿美元,相比较,2018年同期的销售、一般及行政管理费用为4882万美元。销售、一般及行政管理费用的增加主要归因于员工人数的增加,其中包括扩大商业团队规模以支持在中国已上市产品的分销、临床后期候选药物预计在美国和中国的产品发布、以及提高的专业服务费和运营活动发展所需成本的增加。销售、一般及行政管理费用的总体增加还由于与此相关的股票期权费用的增加。截至2019年9月30日的第三季度股票期权费用为1614万美元,相比较,2018年同期的股票期权费用为961万美元。该增加主要是由于员工人数的增长。
净亏损截至2019年9月30日的第三季度的净亏损为3.0736亿美元、或每股0.39美元、或每股美国存托股份(ADS)5.11美元,相比较,2018年同期的净亏损为1.4403亿美元、或每股0.19美元、或每股ADS2.53美元。
财务摘要
简要合并资产负债表摘要数据(美国一般公认会计准则)
(单位为1,000美元)
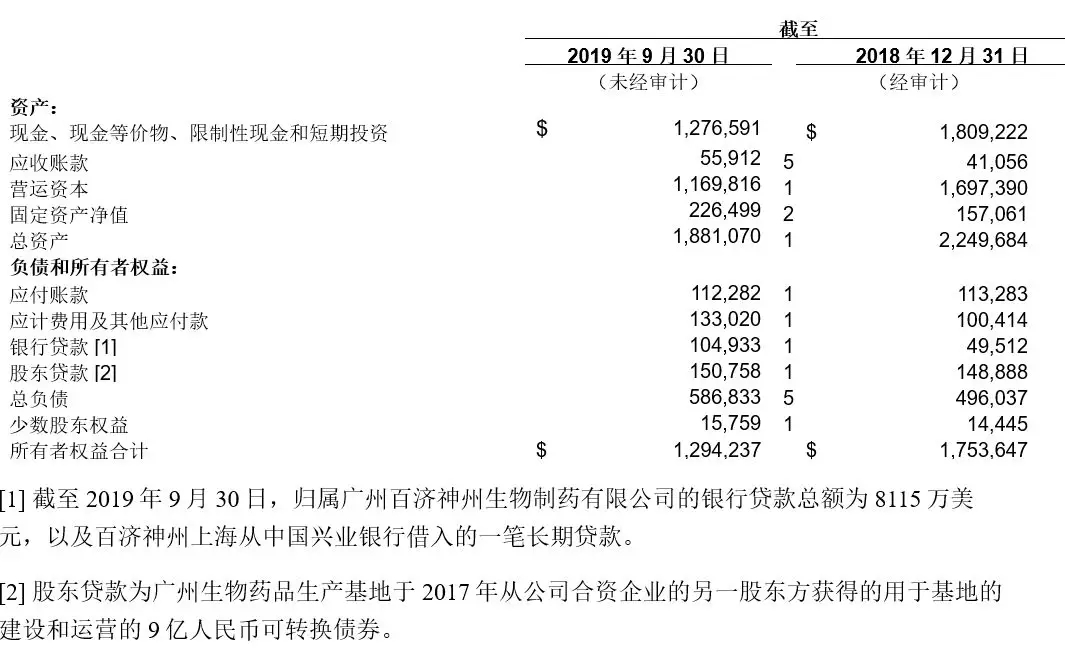
简要合并营运报表(美国一般公认会计准则)
(除普通股数量、ADS数量、每股普通股和每股ADS数据外,单位为1,000美元)
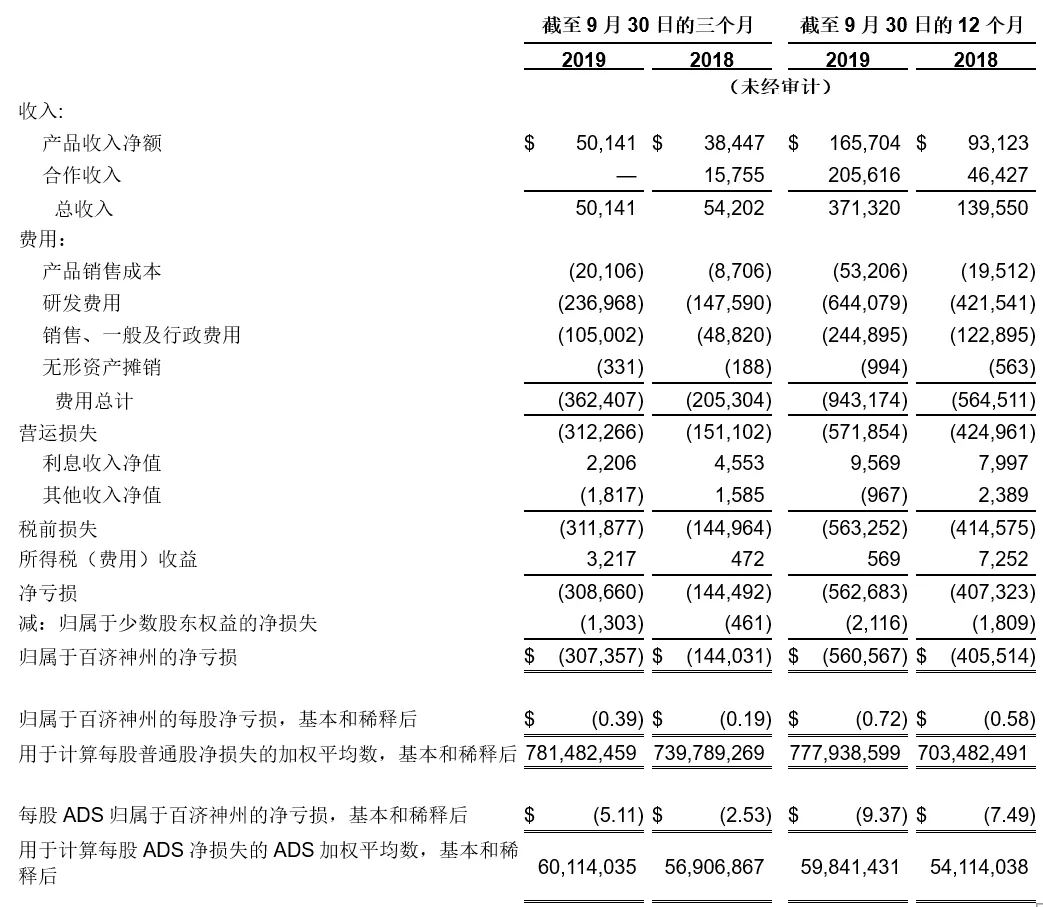
来源于:百济神州